[1] 提供報告基本事項での記入方法
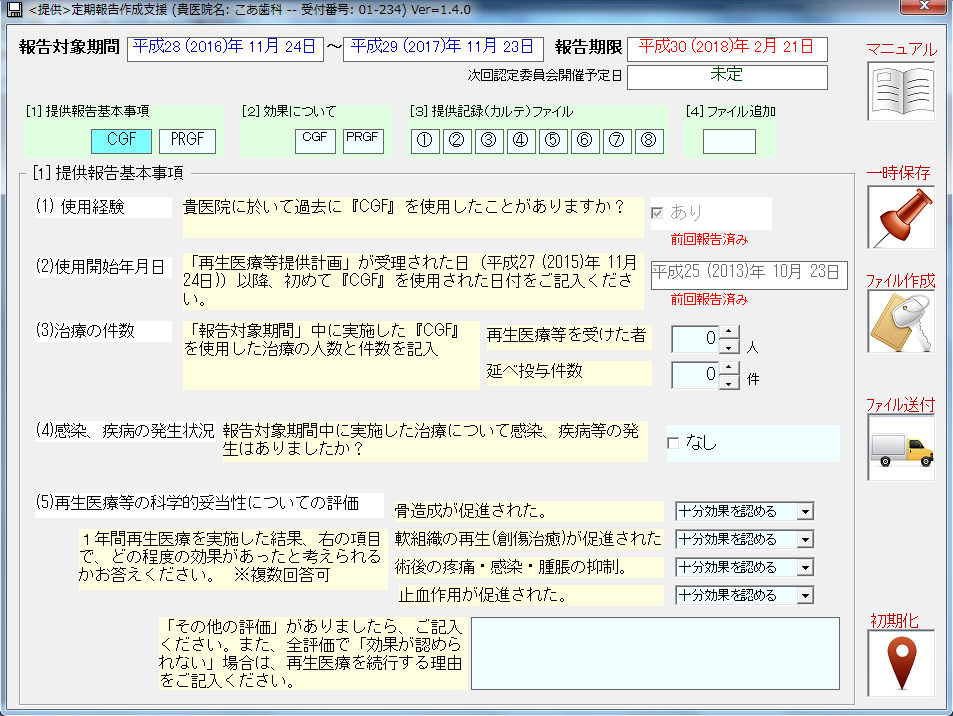
☆基本設定画面☆
立ち上げ直後、上記の画面が表示されます。
医院様においてはまず最初に、画面上バーの「医院名」が正しく表記されていることをご確認ください。
次に、医院様で使用している「加工物数」とメイン画面の「基本事項入力項目数」が一致していることをご確認ください。
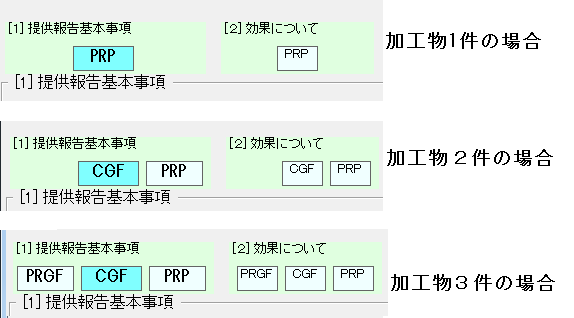
→ 異なる場合は至急ご連絡ください
☆入力項目☆

(1) 使用経験
「過去」にCGF等の加工物を治療で使用したことがあるかどうかを回答ください。
(2) 使用開始年月日
「再生医療提供受理日」以降、CGF等の加工物を使用した開始日をご回答ください。
注)上記(1)(2)は前年度の「提供定期報告」で既にご回答されている場合は以下の様な表示画面となり、
ご回答ができなくなっております。
(3) 治療の件数

「報告対象期間」中に実施した特定細胞加工物を使用した治療の人数と件数を記入します。
※ 件数について
「同一の加工物」を「同一の患者様」に『同時に複数個所』に添付する場合は「1件」
「同一の加工物」を「同一の患者様」に『時期が異なり、採血もやり直した場合』は
同じ治療箇所でも「2件」となります。つまり、治療の件数と採血の回数は同じになります。
よって、「人数」は常に「件数」以下となります。
(4)感染・疾病の発生状況
報告対象期間内で感染や疾病がありましたらチェックし「報告事象発生あり」にしてください。
感染・疾病がない場合はチェックは不要です。
下記画像は感染・疾病がない場合です。
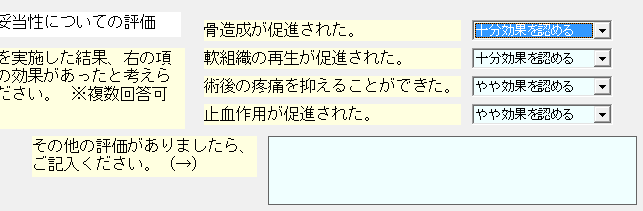
(5)再生医療等の科学的妥当点についての評価
再生医療を実施した結果、どの程度の効果があったか「コンボ選択」して下さい。
詳しい説明は効果選択肢にカーソルを置くと表示されます。(下記画像)